총 17건
-
 강아지 디스크 수술, 최소침습 척추내시경
강아지 디스크 수술, 최소침습 척추내시경
최소침습 척추내시경으로 치료한 강아지 디스크(IVDD)증례 김현호 외과대표원장 [본문 한 눈에 보기] ✅ 갑작스러운 후지마비로 내원한 IVDD 환자에서 MRI로 디스크 탈출을 확인하였습니다. ✅ 양방향 척추내시경을 이용한 Hemilaminectomy 감압수술을 시행하였습니다. ✅ 리본동물의료센터는 척추내시경 경험을 기반으로 정확한 감압수술을 시행하며 환자는 1개월 후 자력보행이 가능해졌습니다. IVDD(Intervertebral Disc Disease)는 개에서 신경학적 이상을 초래하는 가장 흔한 원인 중 하나입니다.(그림1) 그림1. 탈출된 디스크 형태에 따라 다르지만 대부분의 치료는 수술을 통한 감압이 지시됩니다. 감압을 해주는 기법들은 문헌에 따라 조금 다르게 표현되기도 하지만 대표적으로 Hemilaminectomy, Mini-Hemilaminectomy, Pediculectomy 등이 있습니다. (그림2) 그림2. 척추 감압술의 종류 감압술은 일반적으로 피부와 근막을 길게 절개를 하고 spine 주변 muscle을 분리한 뒤 측면을 노출하고 수술이 진행되게 됩니다. 따라서 주변 근육 및 구조물을 필연적으로 손상시키게 되고 이는 술 후 통증과 근 위축 등으로 이어지게 됩니다. (사진1) 사진1. 감압술을 시행하기 위한 절개창 이러한 개방 수술의 단점을 극복하기 위해 수의학에서도 최소 침습 척추수술들이 연구되고 시행이 되어 오고있습니다. 카메라나 현미경을 사용한 최소침습 기법은 적은 조직손상과 확대를 통한 가시화의 장점이 있습니다. 많은 종류의 최소침습 기법이 소개되어져 왔으며, 접근법의 종류에 따라 크게 두가지 형태로 구분됩니다. 첫번째는 tubular retractor를 쓰는 방식이고 두번째는 아에 피부를 관통하여 접근하는 방식입니다. 이러한 큰 틀에서 응용된 다양한 기법들이 있으며, 대표적으로 MED (Micro-endoscopic discectomy)와 PED (Percutaneous endoscopic discectomy)기법이 보고되어 있습니다. (그림3) 그림3. A : MED (Micro-endoscopic discectomy), B : PED (Percutaneous endoscopic discectomy) 하지만 이런 수술은 이 수술법을 위해 고안된 특수한 장비를 사용해야하고 조작의 힘듦으로 인해 수의에서 널리 보급되어 있지는 않은 상황입니다. 아직 수의쪽에서는 적용사례가 거의 없지만 인의쪽에서는 이런 단점들을 극복하여 기존 관절경 장비들을 이용할 수 있고, 두개의 portal을 이용하여 조작이 더 편한 Unilateral biportal endoscopic spine surgery, Biportal Endoscopic spine surgery 이하 (BESS, UBE) 라는 방식도 많이 사용되고 있습니다(그림4). 그림4. Unilateral biportal endoscopic spine surgery, Biportal Endoscopic spine surgery (BESS, UBE). 이런 수술 기법은 1996년 사람의사인 antoni가 고안해내었으며, 2013년 soliman이라는 사람의사가 현재와 유사한 개념의 수술법으로 발전시켰습니다. 2016년부터 한국에서 여러 논문들이 나오며 Biportal라는 용어가 쓰이기 시작했으며 UBE라는 용어가 쓰이기 시작하였습니다. 수의 쪽에서는 유사한 개념의 보고가 2025년에 중국에서 보고된 바 있지만, Full endoscopic surgery보단 assist 개념으로 소개되어 있고, Full endoscopic surgery에 관한 두편의 논문이 한국에서 보고되었습니다. 이번엔 수의학에서 아직 보급되지 않은 UBE 기법을 이용하여 IVDD에서 Hemilaminectomy와 Mini-Hemilaminectomy를 성공적으로 실시한 증례들을 소개하고자 합니다. 첫번째 환자는 9살령 중성화 수컷이었고, 5.5kg으로 비교적 작은 체형의 개였습니다. 증상은 전날 갑작스러운 후지마비 증상을 보여 내원하였고, 내원시에 Grade 5로 deep pain도 소실된 상태였습니다. Mri 검사상 요추 4/5번 좌측으로 디스크 탈출이 확인되었습니다.(사진2) 증상의 정도가 심하여 충분한 감압을 위해 수술은 Hemilaminectomy 를 계획하여 실시하였습니다.(사진3,4) 포트가 장착된 부분에 국소마취 진통제 처치 후 입원 및 수액 처치를 진행하였습니다. 술 중 합병증은 관찰되지 않았으며, 수술 후 신경학적 개선이 관찰되었습니다. 2일차 심부통증이 확인되고, 2주차에 보조하에 보행이 가능해졌으며 한달 뒤 스스로 보행이 가능해졌습니다. 사진3. 척수 아래 디스크를 확인하고 제거 사진4. 디스크 물질들을 모두 제거 후 척수의 주행 사진5. 술부 사진 인의에서 Biportal 기법 또한 다음과 같이 son’s space라고도 하는데, multifidus 머슬의 결사이 틈의 공간(그림5)을 이용하여 진행하게 되는데 이로 인해 근육의 손상을 최소화하게되어 빠른 회복과 기능적인 이점이 대표적인 알려져있습니다. 한 연구에서는 개발수술의 경우 7%의 근육감소를 보이는 반면, 최소침습기법을 이용하면 10%의 근육량 상승을 보여, 결과적으로 17퍼센트의 차이가 발생한다고 해석하기도 합니다. 또 여러 예후 관련 논문들을 meta 분석한 한 연구에서는 UBE와 PED, MED를 비교하였는데,(표1) 결과적으로 최소 침습 기법들끼리 장기적 예후에서 차이는 보이지 않았지만, 초반의 통증 및 기능회복에서 UBE와 PED가 유리함을 시사하였습니다. PED와 UBE에서의 유의미한 차이는 없었습니다. 또한 기존 최소 침습 수술에 비해 양방향 척추 내시경의 장점은 조작의 편의성입니다. 이는 다음과 같이 triangulation 을 형성함에 따라 나오게 됩니다. 다음의 모식도를 보시면 피부에서 이런 Portal 이 들어가며 pivot point 를 형성합니다. 이 지점을 축으로 표1. UBE와 PED, MED 비교 이런 결과와 연구들을 토대로 아직 수의 관련 많은 연구가 필요하지만, 기술적으로 Hemi laminectomy와 Mini-hemilaminectomy가 가능한 점에서 수의 환자에서 척추 감압을 위한 실용적이고 효과적인 최소 침습적 대안이 될 수 있음을 시사합니다. 더 나아가 인의에서와 같이 척추의 안정화나 종양 제거 등도 충분히 가능할 것이라 생각합니다. 저희 리본동물의료센터는 새로운 기술을 그저 빠르게 도입하는 것이 목표가 아닙니다. 철저한 준비와 충분한 검증을 바탕으로 반려동물에게 가장 안전하고 확실한 치료를 제공하는 것이 목표입니다. 그 결과, 영남권 최초로 척추내시경을 도입하여 현재까지도 꾸준히 다양한 케이스를 성공적으로 축적해 오고 있습니다. 철저한 준비아래 쌓은 경험이 실력으로 이어지고, 실력이 곧 반려동물의 회복으로 이어진다는 믿음 아래 항상 한 발 앞서 정확한 치료를 선도하고 있습니다. 저희 리본동물의료센터는 끝까지 책임지는 치료, 그리고 반려동물에게 더 나은 내일을 약속드립니다.
관리자 2026.02.24 -
 강아지 구토 설사 체중감소 - 항문낭종양(AGASACA)
강아지 구토 설사 체중감소 - 항문낭종양(AGASACA)
부산 강아지 항문낭종양 수술 · 항문낭선암 치료 · 항문 종괴 검사 전문, 부산 동래 24시 리본동물의료센터 [본문 한 눈에 보기] ✅ 항문 주변에 만져지는 종괴(혹)가 확인되어 병원에 내원하였으며 검사 결과 항문낭 종양이 의심되었습니다. ✅ 영상검사와 세포검사를 통해 종양을 평가한 뒤 종양이 발생한 항문낭을 제거하는 수술(closed anal sacculectomy)을 시행했습니다. ✅ 전이 없이 완전 절제가 이루어졌으며 수술 후 합병증 없이 회복하여 현재까지 건강하게 생활하고 있습니다. 항문낭종양(AGASACA) 정성호 1. 내원하신 이유 이번 환자는 항문 주변 종괴를 주증으로 내원하였습니다. 항문 주변을 과도하게 핥거나 긁는 행동은 관찰되지 않았고 궤양이나 삼출과 같은 국소 염증 소견도 확인되지 않았습니다. 다만 최근 약 1년 사이 체중이 약 1 kg 감소한 병력이 확인된 상황이었습니다. 1.진단 1) 신체검사 신체검사에서는 직장검사를 포함하여 종괴의 위치, 크기, 형태, 경도 및 가동성을 중점적으로 평가하였습니다. 직장검사상 요추하 림프절의 비대는 확인되지 않았습니다. 항문 주위 종괴의 크기는 약 3 × 3 cm였으며 둥근 형태(round shape)로 관찰되었습니다. 촉진 시 경도가 단단했고 주변 조직과 고정된 상태로 확인되었습니다. 2) 혈액검사 혈액검사는 CT 촬영을 위한 마취 전 전신 상태 평가를 목적으로 시행하였습니다. 일반 혈액검사 및 혈청화학 검사에서 특이 소견은 관찰되지 않았습니다. 추가적으로 혈중 칼슘 농도를 확인하였습니다. 이는 항문 주위 종양 중 악성도가 높은 항문낭종양(apocrine gland anal sac adenocarcinoma)에서 고칼슘혈증이 동반되는 경우가 흔하기 때문입니다. 본 환자의 혈중 칼슘 농도는 정상 범위에 해당하였습니다. 다만, 정상 칼슘 수치가 항문낭종양을 배제하는 것은 아니며, 임상적으로는 영상 검사 및 병리학적 평가가 반드시 필요합니다. 3) 초음파 검사 항문낭 mass 의심 요추하 림프절 비대 보이지 않음 4) CT 검사 우측 항문낭을 감싸고 있는 길이 3.2 cm, 너비 2.3 cm 크기의 mass 확인 mass는 직장의 점막층과 연결성을 보이지 않음 전이 소견 보이지 않음 5) 세포검사 세포질 배경에 맨핵 형태로 보임 anal sac adenocarcinoma이 가장 의심 확진을 위해선 조직검사가 필요함. 2.수술 현재 항문 주변에 확인된 종괴는 신체검사, 혈액검사, 영상검사 결과를 종합했을 때 악성도가 높은 항문낭선암(anal sac adenocarcinoma)이 강하게 의심되는 상황이었습니다. 따라서 항문낭선암에서 추천되는 closed anal sacculectomy를 시행하였습니다. 이때 종양세포를 최대한 제거하기 위해서 근적외선 장비로 종양 확인 및 마진 확보하여 수술 진행 이 수술법은 종양으로 변화된 항문낭을 절개하여 열지 않고, 밀폐된 상태로 완전 절제하는 방법입니다. 이러한 술식을 선택한 이유는, 항문낭을 개방할 경우 종양세포가 수술 부위 및 주변 조직으로 파종될 위험이 있으며, 특히 침습성이 강한 항문낭종양의 특성상 국소 재발 위험을 증가시킬 수 있기 때문입니다. 3. 예후 본 환자는 우려되었던 주요 술후 합병증인 변실금, 항문 협착, 배변 곤란 등의 증상은 관찰되지 않았습니다. 또한 수술 후 회복 과정도 양호하였으며, 현재 퇴원 후 2년 이상 경과한 시점까지 특별한 문제 없이 건강하게 생활하고 있습니다. 항문낭종양의 예후를 평가한 2007년 Journal of Veterinary Internal Medicine(JVIM)에 발표된 연구가 있습니다. 해당 연구에 따르면, 전이가 없는 환자에서는 24개월 이상 생존기간을 보였습니다. 따라서 본 환자는 전반적으로 예후가 매우 양호한 사례로 평가됩니다. 림프절 전이가 흔함. 다만 항문낭선암(anal sac adenocarcinoma)은 초기 진단 시 이미 전이가 동반된 경우가 50–90%에 이를 정도로 전이 빈도가 높은 종양입니다. 전이는 주로 요추하 림프절(sublumbar lymph nodes)에서 가장 흔하게 관찰되며, 그 외 간, 비장, 폐로의 원격 전이는 약 2–15% 정도로 상대적으로 낮은 빈도를 보이는 것으로 보고되어 있습니다. 본 환자는 다행히 진단 당시 전이 소견이 확인되지 않았던 경우였으나, 이처럼 실제 임상에서는 전이가 이미 존재하는 경우가 흔하다면, 앞서 언급한 연구에서처럼 예후가 불량한 경우도 많은 상황에서 과연 수술을 시행하는 것이 적절한가라는 의문을 가지는 분들도 있을 수 있습니다. 이와 관련하여 2023년 Journal of the American Veterinary Medical Association(JAVMA)에 발표된 연구가 있습니다. 해당 연구에 따르면, 림프절 전이가 확인된 항문낭종양 환자에서 수술 시 전이된 림프절을 함께 절제한 경우, 림프절 전이가 없는 항문낭종양 환자와 비교했을 때 생존기간에서 유의미한 차이가 관찰되지 않았습니다. 즉, 림프절 전이가 존재하더라도 적극적인 외과적 절제(원발 병변 + 전이 림프절)를 시행할 경우, 전이가 없는 경우와 유사한 생존 성과를 기대할 수 있음을 시사하는 결과입니다. 따라서 오히려 림프절 전이가 있다면, 적극적인 외과적 개입이 필요하다는 말씀을 드리고 싶습니다. AGASASA란? Apocrine gland anal sac adenocarcinoma는 항문낭에 존재하는 아포크린샘의 선상 세포가 종양성 변화를 일으켜 발생하는 악성 종양입니다. 이 종양은 개 피부종양의 약 2%, 항문 주위 종양의 약 17%를 차지하는 것으로 보고되어 있습니다. 항문낭선암은 침습성이 높고 전이가 비교적 흔한 종양으로 알려져 있으며 현재 가장 권장되는 치료는 종양이 발생한 항문낭 자체를 제거하는 수술적 치료, 즉 closed anal sacculectomy입니다. 이 술식은 종양으로 변한 항문낭을 개방하지 않고 통째로 제거함으로써 국소 종양 조절과 종양세포 파종 위험을 최소화하는 데 목적이 있습니다. 다만 항문낭은 내·외 항문괄약근 사이에 위치해 있기 때문에 수술 과정에서 외항문괄약근이 손상될 경우 변실금이 발생할 수 있는 위험이 있습니다. 그 외에도 수술 부위 누공 형성, 항문 협착과 같은 합병증이 보고되어 있으며 이에 따라 정확한 해부학적 이해와 숙련된 술기가 매우 중요합니다.
관리자 2026.02.09 -
 강아지 고양이 핍뇨가 동반된 급성 신장 손상의 치료법, 이도희 내과과장
강아지 고양이 핍뇨가 동반된 급성 신장 손상의 치료법, 이도희 내과과장
핍뇨가 동반된 급성 신장 손상의 치료법 이도희 내과과장 “급성 신장 손상은 50%의 높은 사망률을 나타내며 특히 핍뇨는 예후와 연관된 중요한 초기 지표입니다. 급성 신장 손상에서 핍뇨를 조기 발견하고 적절한 처치, 모니터링이 이루어져야 합니다.” 급성 신장 손상(acute kidney injury, 이하 AKI)은 다양한 원인에 의해 신장 기능이 갑작스럽게 감소하는 상태로 개와 고양이에서 치사율이 50% 정도로 매우 높습니다. 핍뇨(oliguria)는 AKI에서 중요한 초기 지표로 세뇨관의 기능 상태를 반영하며 과수화, 고칼륨혈증과 같은 합병증과 연관되어 예후와 밀접한 연관이 있습니다. AKI 환자에서 핍뇨의 기전과 치료 전략, 그리고 AKI 환자에서 치료를 위해 고려해야 할 다른 사항들을 소개하고자 합니다. 1. 핍뇨, 무뇨의 정의 개와 고양이에서 정상적인 뇨량은 1-2 ml/kg/hr입니다. 뇨량이 1 ml/kg/hr 미만으로 감소한 경우를 핍뇨(oliguria)라 하며, 이는 절대적 핍뇨(absolute oliguria)에 대한 기준입니다. 뇨량이 정상 범위 내에 있지만 환자의 상태와 필요량 대비 뇨량이 적은 경우를 상대적 핍뇨(relative oliguria)라 하며, 일반적으로 수액 처치를 하는 상태에서도 뇨량이 2 ml/kg/hr 이하인 경우를 상대적 핍뇨라 합니다. 뇨량이 0-0.05 ml/kg/hr인 경우 무뇨(anuria)에 해당합니다. IRIS AKI 가이드라인에 따르면 6시간 이상 뇨량이 1 ml/kg/hr 미만인 상태를 핍뇨라 정의하고 있습니다. 2. AKI에서 핍뇨의 기전 AKI에서 핍뇨는 다양한 기전에 의해 발생합니다. 세뇨관 상피세포가 손상되며 만들어진 세뇨관 원주(cast)가 내강을 막거나 세뇨관의 손상으로 뇨가 내강에서 간질로 빠져나가(tubular backleak) 핍뇨가 발생할 수 있습니다. 또는 신장의 관류 저하로 발생한 사구체 여과율(glomerular filtration rate, GFR) 감소를 보상하기 위해 알도스테론과 항이뇨 호르몬(anti-diuretic hormone, ADH)의 분비가 증가하는데, 이로 인해 원위 세뇨관에서 수분과 sodium의 재흡수가 증가하여 핍뇨가 발생하기도 합니다. 즉, AKI에서 핍뇨는 신장 손상의 증거일 뿐만 아니라 세뇨관-사구체 피드백 기전이 작동하고 있음을 나타내는 지표라고도 볼 수 있습니다. 급성 신장 손상(AKI)에서 핍뇨가 발생하는 기전 핍뇨로 인해 적절한 뇨량이 유지되지 않는 경우에는 과수화와 고칼륨혈증이 발생할 수 있습니다. 따라서 AKI에서 핍뇨와 무뇨가 발생하면 투석 없이 회복의 기회를 상당히 제한시킵니다. 따라서 핍뇨는 AKI 심각도의 지표이자 사망에 대한 중요한 위험 요소 중 하나로 남아있습니다. 3. AKI 환자에서 고칼륨혈증 AKI 환자에서 고칼륨혈증(>5.5 mEq/L)이 흔하나, 7.5 mEq/L 이상의 심한 고칼륨혈증은 흔하지 않습니다. 심한 고칼륨혈증은 신장 실질이 손상된 환자보다 요로계 폐색에 의한 신후성(post-renal) 질소혈증 환자에서 더 흔합니다. 만약 고칼륨혈증으로 인해 심전도상 변화나 심한 서맥이 보인다면 응급 처치로 10% calcium gluconate 0.5-1.5 ml/kg를 정맥으로 천천히 투여해야 합니다(고양이의 경우 3 ml per cat). 심전도상 변화가 없는 안정적인 환자의 경우 regular insulin 0.5 U/kg IV와 인슐린 unit당 2 g dextrose를 정맥 투여할 수 있으며, 또는 1.25-2.5% dextrose를 4-6시간 동안 CRI 적용할 수 있습니다. 만약 투석이 예정되어 있는 환자라면, 투석하는 동안 저칼륨혈증이 발생할 수 있으므로 투석 시작 2~3시간 전에는 고칼륨혈증에 대한 처치를 중단해야 합니다. 4. AKI에서 수액처치 수액처치를 하기 전 다음과 같은 사항을 주의해야 합니다. 먼저, 높은 수액 속도가 사구체 여과율을 증가시키는 것은 아닙니다. 수액 처치의 목적은 관류와 수화 상태를 유지하는 것입니다. 두 번째로, sodium과 chloride의 농도에 주의해야 합니다. 높은 chloride 농도는 사구체 여과율을 감소시키므로, 탈수가 교정된 이후 유지 수액으로는 0.45% NS, 또는 0.45% NS + 2.5% dextrose 적용을 추천합니다. 세 번째로, 가능하면 합성 콜로이드를 피해야 합니다. 합성 콜로이드는 세뇨관 상피세포의 기능을 감소시키고 삼투성 신세뇨관 손상(osmotic nephrosis)을 일으켜 뇨량을 감소시킬 수 있습니다. 환자의 상태와 목적에 따라 다음과 같이 수액을 선택합니다. 1) Resuscitation(소생) : 저혈량증이 있는 환자에서 혈량과 관류를 개선시키기 위한 목적으로 고장성(hypertonic) 또는 등장성(isotonic) 수액을 사용합니다. Lactate ringer solution(LRS), plasmalyte와 같은 등장성의 balanced fluid를 개에서는 10-20 ml/kg, 고양이에서는 5-10 ml/kg를 15분 이상에 걸쳐 bolus 투여합니다. 저혈량증 환자에서 수액을 10분간 bolus 투여했을 때와 20~60분간 투여했을 때 임상적 이점의 차이가 없었다는 보고가 있으므로, 기존에 알려진 것보다 좀더 느린 속도로 투여할 수있습니다. 등장성 수액만으로 안정화되지 않는 경우 고장성 수액인 7% saline 4 ml/kg을 5~10분 이상 투여할 수 있습니다. 1~2번의 crystalloid 수액으로도 개선이 없을 시 신선 냉동 혈장(fresh frozen plasma, FFP)이나 알부민과 같은 natural colloid를 고려할 수 있습니다. 2) Replacement(보충) : 탈수를 교정하고 체액 소실을 교정하기 위해서는 등장성 또는 저장성(hypotonic) 수액을 사용합니다. 구토, 설사, 과도한 뇨량으로 인한 체액과 전해질의 손실을 보충하기 위해 LRS, plasmalyte와 같은 buffered crystalloid를 사용합니다. 배뇨를 통한 저장액의 손실을 보충하기 위해서는 저장성 수액도 사용할 수 있습니다. 3) Maintenance(유지) : 체액을 유지하기 위한 목적으로 저장성 수액을 사용합니다. 이는 우리가 일상적으로 생활할 때 바닷물이 아닌 생수나 이온음료를 먹는 것과 유사합니다. 측정 불가능한 손실(insensible loss)은 호흡, 피부 등을 통해 소실되는 양으로 1 ml/kg/hr로 계산합니다. 측정 가능한 손실(sensible loss)은 뇨와 구토, 설사를 포함합니다. 하루 동안 측정 불가능한 체액량 손실과 측정 가능한 손실량을 합하여 유지 수액 속도를 결정합니다. 예를 들어, 5 kg 강아지에서 하루 뇨량이 220 ml, 구토와 설사량이 약 20 ml였다면, 하루 동안 투여되어야 하는 유지 수액량은 측정 불가능한 손실 1 (ml) * 5 (kg) * 24 (hr)과 측정 가능한 손실량 220 + 20 ml를 합쳐 총 360 ml를 투여해야 합니다. (360 ml/24 hr = 15 ml/hr) 5. 신후성 질소혈증의 배제 AKI라고 판단하기 전 신후성 질소혈증을 배제해야 하며, 특히 고양이는 항상 복부초음파 검사를 통해 요관 폐색과 수신증 여부를 확인해야 합니다. 수액 처치를 받고 있는 고양이라면 신우(renal pelvis) 3.4 mm까지는 정상으로 볼 수 있습니다. 신우가 7 mm 이상이면 요관 폐색 가능성이 높고, 13 mm 이상인 경우에는 요관 폐색으로 판단할 수 있습니다. 요관 폐색이 있어도 신우가 확장되지 않을 수 있으니 있으므로 주의해야 하며, 고양이에서 요관 확장이 보인다면 신우 크기와 관계없이 요관 폐색으로 볼 수 있습니다. 6. AKI 환자에서 고혈압 관리 AKI에서 질소혈증의 심각도와 관계 없이 고혈압이 발생하며, AKI 개의 16%는 고혈압으로 인한 망막병증이 발생합니다. 수축기 혈압 160 mmHg 이하로 유지하는 것이 목표이며, 이를 위해서는 고혈압 치료 뿐만 아니라 통증/불안 조절도 동반되어야 합니다. 과수화가 고혈압을 일으킬 수 있으므로 과수화를 특히 피해야 합니다. 7. 핍뇨 환자에서 수액 처치와 이뇨제 처치 핍뇨 환자에서 수액 처치를 할 때 과수화를 피하는 것이 매우 중요합니다. 핍뇨 환자가 충분히 수화되어 있다면 0.45% NaCl를 투여하며 뇨량의 in/out에 따라 수액 속도를 조절합니다. 핍뇨 환자가 과수화되어 있다면 정맥 수액처치를 중단하고 필요시 이뇨제를 적용할 수 있습니다. 정맥으로 투여되는 수액 뿐만 아니라 정맥 투여 약물, 약물 투여시 플러싱하는 수액, 식이에 포함된 액체량도 포함해야 합니다. 과수화 위험성이 높다면 투석을 고려할 수 있습니다. 핍뇨 환자에서 이뇨제 사용의 indication은 고칼륨혈증과 과수화입니다. 탈수나 저혈량증이 있는 환자에서는 이뇨제 사용을 피해야 합니다. 이뇨제는 핍뇨/무뇨와 AKI를 치료하는 약물이 아니며, 핍뇨로 인해 과수화된 환자를 관리하기 위한 목적으로 사용합니다. 이뇨제로 인해 뇨량이 증가하더라도 이는 사구체 여과율을 증가시키거나 질소혈증을 개선시키지 않습니다. 핍뇨를 다뇨로 전환시키기 위해 furosemide를 1-4 mg/kg, 이후 필요시 6~12시간 간격으로, 또는 0.25-1 mg/kg/h로 6시간까지 투여할 수 있습니다. Furosemide는 알부민에 결합하여 세뇨관 주위 모세혈관에 전달되어 근위세뇨관으로 분비되거나 헨리고리의 NKCC 수용체에 결합하여 작용합니다. 따라서 과수화와 저알부민혈증이 동반된 AKI 환자에서는 이뇨제의 수송 능력이 떨어지고, 요독이 근위세뇨관의 furosemide 분비와 NKCC 수용체와의 결합을 방해하므로 심한 질소혈증 환자에서는 furosemide에 대한 반응성이 떨어집니다. Furosemide의 효과를 예측하기 위해 퓨로세마이드 스트레스 검사(furosemide stress test, FST)를 시행할 수 있습니다. FST는 약물에 대한 효과 뿐만 아니라 신세뇨관의 기능을 예측하는 지표로, FST에 대한 반응이 떨어지는 경우, 투석이 필요한 정도로 심한 AKI로 진행될 가능성이 높습니다. AKI 초기 단계에 있는 혈량이 정상적이고 수화된 개, 고양이에서 요도카테터를 장착한 뒤 furosemide 2 mg/kg를 정맥 투여, 2시간 뒤 뇨량을 측정합니다. 뇨량이 1.5 ml/kg/hr 이상이거나 기존 뇨량의 2배 이상 증가할 시 반응이 있는 것으로 판단합니다. Furosemide 투여 이후 다뇨 상태로 바뀌지 않는다면 더 심한 AKI를 의미하며 투석의 필요성을 나타냅니다. 핍뇨 환자에서 다뇨를 유발하기 위해 만니톨(mannitol)을 사용할 수 있으나 다뇨 상태로 전환되지 않는 경우 과수화와 폐수종의 위험성이 높다는 단점이 있습니다. 사람 가이드라인에서는 AKI 환자에서 만니톨을 사용하지 않으며, 핍뇨/무뇨 환자에서 만니톨의 반복 사용은 피하는 것이 좋습니다. 만약 사용해야 한다면 만니톨 0.25-1 g/kg을 15~20분 이상, 4~6시간 간격으로 투여하거나 0.06-0.12 g/kg/hr로 CRI 투여합니다. 고칼륨혈증을 유발할 수 있으니 전해질을 모니터링해야 합니다. 8. 핍뇨 환자의 모니터링 핍뇨 환자에서 매일 PCV, 혈중 총단백질, 신장수치, 혈당, lactate 농도를 평가하는 것이 좋습니다. 체온, 심박수, 호흡수, 혈압은 6~8시간 간격, 체중과 뇨량은 4~6시간 간격으로 평가합니다. 일정한 상태에서 체중을 측정할 수 있도록 체중 측정 전 걷게 하여 배뇨를 유도하고 뇨팩을 비우며, 복수 등 체강내 삼출물의 무게를 고려해야 한다. 고칼륨혈증 위험이 있을 시에는 심전도 모니터링이 권장됩니다. 9. 혈액투석 기존 내과적 관리에 반응하지 않고 질소혈증이 심해지는 경우, 고칼륨혈증이나 산증이 심한 경우, 핍뇨/무뇨, 과수화 상태에 있는 AKI 환자에서는 투석이 지시됩니다. 투석을 했을 때에도 AKI 환자에서 회복률은 40~50%, 만성 신장 질환에서 급성 악화(Acute on Chronic Kidney Disease, ACKD) 환자에서 회복률은 40%로 알려져 있습니다. 10. 결론 AKI 환자에서 핍뇨는 중요한 초기 지표로 조기 발견과 적절한 모니터링, 처치가 이루어져야 합니다. 정맥 수액 처치는 환자의 상태에 맞추어 조절하며 과수화를 피해야 합니다. 뇨제가 신장 질환을 치료하지는 않지만 과수화를 조절하는 데에 도움을 줍니다. 핍뇨 상태의 AKI 환자에서 기존 내과적 처치에도 개선이 없는 경우 투석이 지시됩니다. Reference 1. Keir I, Kellum JA. Acute kidney injury in severe sepsis: pathophysiology, diagnosis, and treatment recommendations. J Vet Emerg Crit Care (San Antonio). 2015;25:200-9. 2. Langston C, Gordon D. Effects of IV Fluids in Dogs and Cats With Kidney Failure. Front Vet Sci. 2021;8:659960. 3. McCance KL, Huether SE. Pathophysiology: The biologic basis for disease in adults and children. 9th ed. St. Louis: Elsevier, 2018. p.1364. 4. Thoen ME, Kerl ME. Characterization of acute kidney injury in hospitalized dogs and evaluation of a veterinary acute kidney injury staging system. J Vet Emerg Crit Care (San Antonio). 2011;21:648-57. 5. Troìa R, Gruarin M, Grisetti C, et al. Fractional excretion of electrolytes in volume-responsive and intrinsic acute kidney injury in dogs: Diagnostic and prognostic implications. J Vet Intern Med. 2018;32:1372-1382.
관리자 2026.02.06 -
 강아지 요실금 - 방광결석 및 요도결석
강아지 요실금 - 방광결석 및 요도결석
[본문 한 눈에 보기] ✅ 나이가 많은 강아지가 소변이 계속 새는 요실금 증상으로 내원했으며 영상검사에서 방광과 요도에 다수의 결석이 확인되었습니다. ✅ X-ray와 초음파 검사 후 방광절개술과 요도 플러싱을 통해 결석을 제거하고 방광 내부를 방광경으로 확인했습니다. ✅ 결석은 재발 위험이 높은 질환으로 수술 후에도 정기적인 영상검사와 수분 섭취·식이 관리가 중요합니다. 1. 어떤 증상으로 내원했나요? 이 아이는 원래 실외 배변만 하던 아이였는데 약 6개월 전부터 집 안에서 소변을 흘리기 시작해 병원에 내원했습니다. 누워 있는 상태에서도 소변이 새어 나오는 양상 집 안 여기저기에 소변이 계속 떨어져 있는 요실금(incontinence) 산책을 나가면 소변 양은 오히려 많고 집에서는 조금씩 계속 새는 형태 처음에는 혈뇨는 없었고 최근에는 기저귀에 아주 소량의 피가 묻어 나오는 정도 16살의 노령견이고, “소변을 참지 못하고 계속 새는 증상” 때문에 처음 내원하셨다가 이번에 증상이 지속·악화되어 다시 평가를 진행하게 된 케이스입니다. 2. 진단 과정 이번 내원에서 진행한 주요 검사들은 다음과 같습니다. 1.영상 검사 X-ray 방광(bladder) 부위에 다수의 방광결석(cystolith)이 의심되는 음영이 확인되었습니다. Abdominal ultrasound(복부 초음파) bladder wall(방광벽)이 두꺼워져 있어 chronic cystitis(만성 방광염)을 의심할 수 있는 소견 bladder 안에 다수의 결석(cystolith)이 확인되었고, urethra(요도) 방향으로도 여러 개의 결석이 내려가 있는 상태가 확인되었습니다. 2.혈액 검사 CREA, PHOS 상승은 현재 뚜렷하게 관찰되지 않아, 당장은 심한 postrenal azotemia 상태는 아니나,urethra가 결석으로 막히는 급성 폐색이 발생하면 postrenal azotemia로 빠르게 진행할 수 있어 주의가 필요한 상황입니다. 3. 감별 진단 현재 영상·혈액 소견을 종합했을 때 Urinary cystitis + bladder/urethral urolithiasis(방광염 + 방광/요도결석)에 의한 요실금, stranguria(배뇨곤란) 가능성이 가장 크게 확인되었습니다. 3. 치료 과정 수술적 교정 초음파에서 bladder 내 다수의 방광결석,urethra 쪽으로 내려간 결석들,bladder wall 비후(방광염 소견)가 동시에 확인되었습니다. 이로 인해 요실금(incontinence)Stranguria, 반복적인 요로감염 위험이 높은 상태로 판단되어 → bladder 및 urethra 결석 제거를 위한 수술(cystotomy + urethral flushing)을 시핼하였습니다. 먼저 배 중앙선으로 작은 절개(midian laparotomy)를 내고 복강에 들어가 bladder(방광)를 조심스럽게 꺼낸 뒤 젖은 거즈로 주변 장기들과 부드럽게 분리해 주었습니다. 그런 다음 bladder apex(방광 끝부분)에 실을 걸어 위로 들어 올려 결석 제거와 봉합이 잘 보이도록 수술 시야를 확보했습니다. Bladder의 아랫부분(ventral surface)에 세로 방향으로 작은 절개를 내는 ventral cystotomy를 시행했습니다. 절개 양쪽에 실을 걸어 입구를 살짝 벌려 준 뒤 bladder 안쪽으로 들어가 다수의 cystic calculi(방광 결석)가 들어 있는 것을 직접 확인했습니다. Bladder 안과 trigone(방광 삼각부), ureter가 열리는 부위까지 잘 보이도록 한 상태에서, 작은 카메라인 cystoscope(방광경)을 절개창을 통해 넣어 bladder 안쪽 점막과 proximal urethra(방광 쪽 요도)를 자세히 관찰했습니다. 이 과정에서 눈에 잘 안 띄는 작은 결석과 동반된 염증·폴립 같은 병변이 있는지도 함께 확인했습니다. 또한 결석이 urethra 쪽으로 떨어졌을 가능성에 대비해, urethral catheter를 넣고 방광 쪽으로 물을 흘려 보내는 flushing을 여러 번 시행하여, urethra 안에 남아 있을 수 있는 결석까지 최대한 씻어 내도록 했습니다. 결석 제거가 끝난 뒤에는 방광경으로 다시 한 번 bladder 안 전체를 확인해 남아 있는 결석이 없는지 꼼꼼히 검사했습니다. 그 다음 bladder wall의 튼튼한 층(submucosa)을 잘 포함하도록 봉합사로 촘촘히 맞대어 봉합한 후, 최종적으로 방광 벽을 통해 주사기로 멸균 생리식염수를 주입하여 방광 내 압력을 올린 뒤, 절개선과 봉합 부위에서 누출이 없는지 확인하는 leakage test를 시행했습니다. 수술 직후 x-ray를 통해 수술 전 확인되었던 urolith가 완전히 제거되었는지 확인했습니다. 4. 예후 1. 수술을 진행하는 경우 bladder는 치유가 매우 빠른 장기라 mucosa 손상은 약 5일,full-thickness 손상은 14–21일 사이에 정상 강도에 가까운 회복이 가능합니다. 수술후 uroabdomen(복강 내 소변 누출) 같은 심각한 합병증은 낮은것으로 보고됩니다. 수술 후 hematuria, dysuria는 약 절반에서 나타날 수 있지만 대부분 수일 내에 자연 호전되는 경향이 있습니다. 2. 수술을 미루거나 하지 않는 경우 현재처럼 bladder와 urethra 내에 결석이 다수 존재하면, 어느 시점에 urethral obstruction(요도 폐색)이 갑자기 발생할 수 있습니다. 요도 폐색이 생기면 bladder가 급격히 팽창하고, postrenal azotemia, hyperkalemia가 생기면서 구토, 무기력, 식욕부진, 심한 경우 생명을 위협하는 상황까지 진행할 수 있습니다. 3. 재발에 대한 예후 bladder urolithiasis는 특히 개에서 “재발률이 높은 질환”입니다. 한 번 방광결석이 있었던 아이들은 최소 3–6개월 간격으로 X-ray·초음파를 통해 재발 여부를 체크하고, 물 섭취량 관리, 체중 관리, 적절한 처방식 유지가 중요합니다. 질병소개 – 방광결석(bladder urolithiasis)이란? 1.방광결석이란 무엇인가요? urolithiasis는 urinary tract(신장, 요관, 방광, 요도) 안에 돌(결석)이 생기는 질환이고,그 중 bladder는 가장 흔하게 결석이 생기는 위치입니다. 결석은 하나의 mineral로만 이루어지기도 하고,층을 이루거나 혼합 구조를 가지는 경우도 있습니다. 2. 어떤 종류의 결석이 있나요? 개와 고양이에서 가장 흔한 두 가지는 Struvite, calcium oxalate 입니다. 그 밖에 urate, calcium phosphate, silica, xanthine, cystine, mixed urolith 등이 드물게 보고됩니다. 3. 어떤 증상이 나타나나요? hematuria(혈뇨)pollakiuria(자주 소변 봄),stranguria/dysuria(배뇨 시 힘주기, 아파함),소변을 참지 못하고 조금씩 새는 요실금(incontinence), urethral obstruction이 있으면 무기력, 식욕부진, 심한 경우 쇼크까지 진행합니다. 4. 어떻게 진단하나요? Urinalysis, urine culture , pH, crystal 형태, 세균 유무를 보고 결석 종류를 예측하고,동반된 urinary tract infection을 확인합니다. 방사선 검사를 통하면 대부분의 struvite, calcium oxalate는 X-ray에서 잘 보일수있으나 urate, cystine 등 일부 결석은 X-ray에 잘 안 보일 수 있습니다. 즉, 잘보이지 않는 결석까지 제거해주는 것이 중요합니다. 5. 치료 방법 결석의 크기, 개수, 위치, stone type, 아이의 전신 상태에 따라 선택합니다. struvite, urate, cystine 일부는 특수 식이와 약물로 녹이는 것이 가능하나 Surgical cystotomy는 가장 전통적이고 많이 시행되는 방법으로 bladder를 여는 수술을 통해 결석을 모두 꺼내고 수술 중에는 cystoscope(방광경)을 이용해 bladder 안쪽 점막과 urethra 입구 근처까지 직접 보면서, 눈에 잘 보이지 않는 작은 결석이나 염증, 종괴가 남아 있지 않은지 확인하는 과정이 매우 중요합니다. 또한 urethral flushing(요도 플러싱)을 반복해서 시행해 urethra 안에 숨은 작은 결석까지 최대한 씻어 내야, 수술 후 요도 폐색이나 결석 재발 위험을 줄일 수 있습니다. 6. 재발 예방 urolithiasis는 재발률이 높기 때문에, 결석을 제거한 뒤가 더 중요합니다. stone type에 따라 다르지만, 공통적으로 물 섭취량을 늘려 urine을 묽게 유지하고,체중·비만을 관리하며,적절한 처방식을 꾸준히 급여하는 것이 필요합니다.
관리자 2026.02.05 -
 이영재 대표원장, 특발성 전정질환과 안면신경 마비 – 대표적인 말초 신경 질환의 병발과 임상적 이해
이영재 대표원장, 특발성 전정질환과 안면신경 마비 – 대표적인 말초 신경 질환의 병발과 임상적 이해
특발성 전정질환과 안면신경 마비 – 대표적인 말초 신경 질환의 병발과 임상적 이해 대표원장 이영재 1. 서론 개에서 급성으로 발생하는 신경학적 이상은 중추신경계와 말초신경계 질환으로 구분할 수 있으며 그중에서도 대표적인 말초 신경 질환으로 특발성 전정질환(Idiopathic Vestibular Syndrome, 이하 ‘IVS’)과 특발성 안면신경 마비(idiopathic facial paralysis, 이하 ‘IFP’)가 있습니다. 두 질환 모두 갑작스럽게 증상이 시작되고, 진행성 경과를 보이지 않으며, 비교적 안정적인 예후를 가진다는 공통점이 있습니다[1,2]. 임상적으로 이 두 가지 질환은 각각 별개로 발생하기도 하지만, 동일 환자에서 동시에 관찰되는 경우도 적지 않습니다. 실제로 말초 전정증후군 환자의 상당수에서 동측의 IFP가 함께 보고되었으며, 반대로 IFP 환자에서도 전정 증상이 동반되는 경우가 흔히 확인되었습니다[3–5]. 이러한 병발 양상은 우연이라기보다는, 말초 전정계와 안면신경이 해부학적으로 매우 인접한 구조라는 점에서 원인을 추정할 수 있습니다. 전정 증상을 보이는 환자에서는 말초성과 중추성을 구분하는 것이 예후와 치료 방향 결정에 매우 중요합니다. 그러나 신경학적 검사만으로 병변 위치를 정확히 판단하는 데에는 한계가 있으며, 실제로 신경학적 국소화와 MRI 진단이 일치하지 않는 경우가 반복적으로 보고되었습니다. 한 연구에서는 신경학적으로 말초성으로 판단된 환자 중 약 30%만이 MRI에서 실제 말초 병변을 보였고, 중추성으로 판단한 경우에도 MRI 일치율은 약 60% 수준에 불과했습니다[6,7]. 본 글에서는 임상에서 가장 흔히 접하게 되는 두 대표적인 말초 신경 질환인 IVS와 IFP를 중심으로, 감별이 필요한 주요 질환들과 이를 임상적으로 어떻게 이해하고 접근해야 하는지를 근거 중심으로 정리해보고자 합니다. 2. 전정계와 안면신경의 해부학 그림 1. 말초 전정계와 안면신경의 해부학적 관계 전정와우신경(CN VIII)과 안면신경(CN VII)은 내이도에서 인접하게 주행하며, 이후 안면신경은 중이 구조와 밀접한 관계를 유지합니다. 이러한 해부학적 특성은 전정 증상과 안면신경 마비의 병발을 설명하는 중요한 구조적 배경입니다. (출처: Veterinary Clinics of North America Small Animal Practice 42(6):1109–26) IVS와 IFP의 병발은 말초 신경계의 해부학적 구조를 이해하면 비교적 자연스럽게 설명됩니다. 말초 전정계는 내이(inner ear)에 위치하며, 반고리관, 전정기관, 달팽이관, 그리고 전정와우신경(CN VIII)으로 구성되어 있습니다[8] (그림 1). 전정와우신경(CN VIII)은 내이도를 통해 두개강 내로 진입한 후, 연수(medulla oblongata)의 등쪽가쪽에 위치한 전정핵(vestibular nuclei)으로 연결됩니다(그림 2). 이 과정에서 전정와우신경(CN VIII)과 안면신경(CN VII)은 하나의 경막초(뇌신경을 싸고 있는 막) 안에서 내이도(internal acoustic meatus)를 함께 통과하며 매우 근접해 있습니다[9,10]. 안면신경(CN VII)은 안면신경관을 따라 주행하며 중이 및 내이 구조와 인접해 있습니다. 이런 해부학적 특징으로 인해 내이 또는 신경관 내에서 발생한 염증이나 부종은 인접 신경으로 파급될 수 있으며 특히, 좁은 골성 신경관 내를 주행하는 안면신경은 경미한 부종에도 쉽게 압박됩니다. 이런 이유로 전정 증상은 비교적 빠르게 호전되는 반면, IFP는 회복이 지연되거나 잔존하는 경과를 보일 수 있습니다[4,11–13]. 그림 2. 중추 전정계와 안면신경의 해부학 전정와우신경(CN VIII)은 연수의 등쪽가쪽(dorsolateral)에 위치한 전정핵(vestibular nucleus, 빨간색)으로 연결되며, 해당 전정핵은 소뇌의 타래결절엽(flocculonodular lobe)과 함께 중추 전정계를 구성합니다. 안면신경(CN VII)의 운동핵(파란색)은 전정핵과 해부학적으로 인접한 위치에 존재하며, 이러한 근접성은 전정 증상과 안면신경 마비가 함께 관찰될 수 있는 해부학적 근거를 제공합니다. (출처: Comparative Veterinary Anatomy: A Clinical Approach, 2022, pp. 181–187) 3. 해부학적 인접성이 만드는 임상 양상 – IVS와 IFP의 병발 IVS와 IFP가 함께 관찰되는 경우는 흔히 볼 수 있습니다. 말초 전정증후군 환자의 약 30–40%에서 같은 방향의 IFP가 동반되었다는 보고가 있으며, 반대로 IFP 환자의 절반 이상에서 같은 방향으로 전정 증상이 함께 관찰되었다는 연구도 보고되어 있습니다[3–5]. 임상적으로 두 증상이 병발된 경우, 전정 증상은 대부분 증상이 급성이며 사경이나 안진 등의 증상이 뚜렷해 보호자가 쉽게 인지하지만 IFP는 전정 증상에 가려져 초기에 병발을 인지하지 못하는 경우가 많습니다[2,5]. 그림 3. 안면신경(CN VII) 마비와 전정 증상이 병발된 코커스파니엘. 좌측 사경(head tilt)과 함께 동측 안면에서 눈꺼풀과 입꼬리의 처짐이 확인됩니다. 또 하나의 중요한 특징은 증상의 회복 속도 차이입니다. 두 질환의 병발 사례에서 전정 증상은 대개 수일 이내에 호전 양상을 보이며, 보행 실조와 안진이 점차 감소하였습니다. 반면 앞서 말한 해부학적 특징 때문에 IFP는 회복이 느리거나, 일부 환자에서는 장기간 잔존해서 편측 안면근육위축과 같은 후유증이 남는 경우도 보고되었습니다[11–13]. 중요한 점은 이러한 병발이 관찰되더라도, 대부분의 경우 임상 경과는 비진행성이라는 점입니다. 병발 자체가 예후 불량을 의미하지는 않으며, 오히려 병변이 말초 신경계에 국한된 경우에는 안정적인 경과를 보이는 경우가 많았습니다[1,3]. 따라서 병발 여부 자체보다는, 정신 상태 변화, 자세 반응 이상, 수직성 안진과 같은 중추 신경계 이상 소견이 동반되는지가 예후 판단에 더 중요합니다[6,7]. 이러한 근거들을 종합해 볼 때, IVS와 IFP의 병발은 새로운 질환 개념이라기보다는, 말초 전정계와 안면신경이라는 해부학적 인접 구조가 큰 영향을 주는 형태로 이해할 수 있습니다. 4. 단독으로 발생하는 특발성 전정질환 특발성 전정질환(Idiopathic Vestibular Syndrome, 이하 ‘IVS’)은 말초 전정계 질환 중 가장 흔한 형태로, 주로 중·노령견에서 급성 또는 초급성으로 발생합니다[1,2]. 사경, 전정성 보행 실조, 안진, 구토가 주요 증상이며, 대부분의 환자에서 정신 상태는 정상으로 유지됩니다. 4.1 진단적 접근 IVS는 전형적인 배제 진단입니다. 신경학적 검사에서 수평성 또는 회선성 안진, 자세 반응(postural reactions)은 정상적이나 전정성 보행 실조만 보이는 말초 전정계 증상을 특징으로 하며 MRI에서 중추성 병변이나 중이·내이염이 배제될 경우 최종적으로 진단할 수 있습니다[2,6]. 일부 환자에서 내이의 액체 신호 변화와 같은 비특이적 MRI 소견(FLAIR 영상에서 내이 액체의 비정상적 고신호나 T2 신호의 비대칭성)이 보고되었으나, 이러한 소견이 예후를 예측하거나 치료 방향을 바꾸는 근거가 되지는 않았습니다[14,15]. 4.2 치료 전략과 약물 사용 IVS의 치료는 대증 치료와 보조적 관리가 중심입니다. 구토, 현훈으로 인해 섭식이 어려운 경우 항구토제, 위장관 보호제, 수액 치료가 임상적으로 도움이 될 수 있습니다[1,2]. 스테로이드의 사용에 대해서는 명확한 근거가 부족하며 투여가 권장되지 않습니다. 여러 연구에서 IVS 환자에서 스테로이드 투여가 회복 속도나 예후를 유의하게 개선했다는 근거는 없습니다[1,16]. 다만, 임상적으로 심한 구토나 현훈이 동반되어 전신 상태 유지가 어려운 경우에는, 항구토제나 진정 효과를 기대한 보조적 약물 사용이 제한적으로 고려될 수 있습니다. 이 경우에도 질환의 자연 경과가 비진행성임을 보호자에게 충분히 설명하고, 약물 사용의 목적이 질환의 “치료”가 아니라 “증상 완화”임을 명확히 안내하는 것이 중요합니다[2]. 대부분의 환자에서 48–72시간 이후부터 자연적인 호전이 관찰되며, 수주 내 기능적 회복이 이루어집니다. 일부 환자에서 사경이 잔존할 수 있으나, 거의 대부분 일상생활에는 큰 영향을 주지 않습니다[2,3]. 그림 4. 정상 개의 T2 강조 MRI 영상 말초 전정계에 해당하는 내이는 정상적으로 액체로 채워져 있어 T2 강조 영상에서 균일한 고신호(하얀색)로 관찰되며, 형태상 흔히 ‘오리???? 모양’으로 표현됩니다. 반면 공기가 차 있는 중이(고실)는 무신호(저신호)로 나타납니다. 전정핵은 MRI 상에서 뚜렷한 경계로 구분되지는 않지만 연수(medulla oblongata)의 dorsolateral에 위치합니다. 임상적으로 말초성 전정 증상을 보이면서 이러한 MRI 소견상 뚜렷한 이상이 확인되지 않는 경우, 다른 원인 질환이 배제되었다면 특발성 전정질환을 의심할 수 있습니다. 5. 단독으로 발생하는 특발성 안면신경 마비 특발성 안면신경 마비(idiopathic facial paralysis, 이하 ‘IFP’)는 안면신경(CN VII)의 단독 침범으로 발생하는 대표적인 말초 뇌신경 질환입니다[4,5]. 입술 처짐, 귀 하수, 눈 깜빡임 감소, palpebral reflex 소실이 특징적인 임상 소견입니다. 5.1 진단적 접근 진단을 위해서는 중이·내이염, 외상, 중추성 병변을 우선적으로 배제해야 합니다. MRI에서는 안면신경의 조영증강이나, 안면신경이 지배하는 근육(특히 caudal digastric muscle)에서 신호 변화 또는 위축이 비교적 높은 빈도로 보고되었습니다[11–13]. 이러한 소견은 IFP가 단순한 기능 이상이 아니라, 염증성 또는 면역매개성 신경병증일 가능성을 시사합니다. 5.2 치료 전략과 약물 사용 IFP의 치료에 대해서는 아직 명확한 표준 치료 지침이 확립되어 있지 않습니다. 일부 증례 보고와 후향적 연구에서 스테로이드가 사용된 경우가 있으나, 스테로이드가 회복률이나 회복 속도를 유의미하게 개선시켰다는 근거는 부족합니다[4,12]. 그럼에도 불구하고, MRI에서 안면신경의 조영증강이 뚜렷하게 관찰되거나, 급성 염증성 신경병증이 의심되는 경우에는 항염 용량의 스테로이드를 제한적으로 고려할 수는 있습니다. 이 경우에도 스테로이드의 투여 목적은 신경 부종 감소를 통한 2차 손상의 최소화이며 단기적으로만 투여합니다[12,13]. 다만 이러한 접근은 근거 수준이 높지 않다는 점을 인지한 상태에서 신중히 판단되어야 합니다. 기타 면역억제제나 항바이러스제의 투여 역시 현재까지는 근거가 부족합니다[5]. 따라서 대부분의 경우 치료의 핵심은 경과 관찰과 보존적 관리입니다. 특히 눈 깜빡임이 감소하며 발생하는 각막 건조, 각막염, 각막 궤양 예방이 매우 중요합니다. 인공눈물, 안연고, 물리적 각막 보호는 거의 모든 환자에서 적극적으로 적용해야 합니다[5]. 예후는 보고에 따라 다양하지만 약 30–60%의 환자에서 완전 회복을 보이고 상당수의 환자는 부분적으로만 회복되거나 안면 비대칭, hemifacial contracture와 같은 후유증이 영구적으로 남을 수도 있습니다[4,5,12,13]. 6. IVS와 IFP의 감별진단 – ‘특발성’으로 진단하기 전에 반드시 배제해야 할 질환들 IVS와 IFP는 모두 배제 진단(diagnosis of exclusion)입니다. 즉, 다른 원인 질환을 충분히 배제한 이후에만 진단할 수 있습니다. 따라서 이 두 질환을 이해하는 데 있어 가장 중요한 과정은 “무엇을 먼저 의심하고, 어떻게 배제할 것인가”입니다. 6.1 중이·내이염 중이염과 내이염은 전정 증상과 IFP를 동시에 유발할 수 있는 가장 흔한 원인 질환 중 하나입니다. 말초 전정계와 안면신경은 해부학적으로 중이와 밀접하게 연결되어 있어, 외이염에서 시작된 염증이 중이와 내이로 확장되면서 두 신경에 동시에 영향을 미칠 수 있습니다[4,10]. 임상적으로는 통증, 외이도 병변, 고막 이상, Horner 증후군 동반 여부 등이 중요한 감별 포인트가 됩니다. 영상 검사에서는 CT 또는 MRI에서 고실(bulla) 내 연부조직 음영 증가나 내이 구조 변화가 확인될 수 있습니다[8,9](그림 5). 이러한 소견이 확인되는 경우에는 특발성 질환보다는 감염성 또는 염증성 질환으로 접근하는 것이 타당합니다. 그림 5. 중이염과 내이염이 병발한 개의 FLAIR MRI 영상. 양측 고실과 내이에서 비정상적인 고신호가 관찰되며, 이는 정상적으로 FLAIR에서 저신호를 보이는 내이 액체와 대비되는 소견입니다. 6.2 중추성 전정질환 중추성 전정질환은 뇌줄기 또는 소뇌 병변에 의해 발생하며, 말초성 질환에 비해 예후가 불량한 경우가 많습니다. 대표적으로 수막뇌염, 뇌경색, 뇌종양 등이 있으며 전정 증상이 관찰될 경우 항상 중추성 병변의 가능성을 염두에 두어야 합니다[6,7]. 중추성 병변을 시사하는 임상 소견으로는 정신 상태 변화, 자세 반응 이상, 수직성 안진, 체위에 따라 방향이 변하는 안진, 다발성 뇌신경 이상 등이 있습니다. 특히 IFP와 전정 증상이 함께 있으면서 이러한 소견이 동반된다면, 말초성 병변만으로 설명하기는 어렵습니다[6,17]. MRI는 중추성 전정질환을 감별하는 데 가장 중요한 검사이며, 신경학적 신체검사만으로는 병변 위치를 정확히 예측하기 어렵다는 점이 여러 연구를 통해 반복적으로 보고되었습니다[6,7](그림 6). 그림 6. 안진이나 보행 이상 없이 좌측 사경을 보이는 개의 MRI 영상 신체검사에서 안진이나 뚜렷한 보행 이상이 없는 경우, 전정 이상에 대한 국소화는 제한적입니다. 본 환자에서는 조영증강 T1 MRI에서 연수 좌측 복외측 부위의 수막종(meningioma)이 확인되었으며, 전정 증상의 원인이 중추성임을 알 수 있습니다. 6.3 내분비 및 대사성 질환 갑상선 기능저하증은 개에서 다양한 비특이적인 신경증상을 유발할 수 있으며 IFP와 전정 증상 모두 보고된 바 있어 스크리닝 차원에서 T4 호르몬의 측정은 반드시 이뤄져야합니다. 다만 갑상선 수치 이상이 확인되었다고 해서, 이를 전정 증상이나 IFP의 단일 원인으로 단정하는 것은 주의가 필요합니다. 임상 증상과 영상 소견을 함께 고려한 종합적인 해석이 중요합니다. 6.4 외상 및 의인성 손상 측두부 외상, 교통사고, 낙상 등은 내이 구조나 안면신경에 직접적인 손상을 유발할 수 있습니다. 또한 중이염의 치료로 시행하는 TECA-LBO (Total Ear Canal Ablation and Lateral Bulla Osteotomy) 이후 합병증으로 전정 증상이나 IFP가 발생하는 경우도 보고되어 있습니다[10]. 이러한 경우에는 병력 청취가 감별에서 매우 중요하며, 증상의 급성 발현 시점과 외상 또는 수술 이력 사이의 시간적 연관성을 반드시 확인해야 합니다. 6.5 다발성 말초 신경병증 및 전신성 신경 질환 급성 다발성 말초 신경병증에서는 안면신경을 포함한 여러 말초 신경이 동시에 이상을 보일 수 있습니다. 이 경우 IFP나 전정 증상이 단독으로 나타나기보다는, 전신적인 근력 저하, 반사 감소, 보행 장애가 함께 관찰되는 경우가 많습니다[19]. 따라서 국소적인 전정 증상이나 IFP가 아닌, 전신적인 신경학적 이상이 동반된다면 단일 말초 신경 질환보다는 전신성 신경 질환을 우선 고려해야 합니다. 7. 글을 마치며 IVS와 IFP는 개에서 가장 흔히 접하게 되는 대표적인 말초 신경 질환입니다. 두 질환 모두 급성으로 증상이 시작되지만 진행성 경과를 보이지 않으며, 비교적 좋은 예후를 가진다는 공통점이 있습니다[1,2]. 다만 급성 발병 시 나타나는 전정증상은 비자발적 안구 움직임이나 균형 상실로 인해 보호자들이 발작이나 경련으로 오인하는 경우가 많으며, 이로 인해 실제 질환의 예후에 비해 초기 내원 시 보호자의 불안 수준이 과도하게 높아지는 경향을 보입니다. 이 두 질환은 단독으로 발생할 수 있을 뿐 아니라, 동일 환자에서 함께 관찰되는 경우도 적지 않습니다. 말초 전정계와 안면신경이 내이도와 신경관을 공유하는 해부학적 구조를 이해한다면, 전정 증상과 IFP가 동시에 관찰되더라도 이를 곧바로 중추성 병변이나 예후 불량으로 해석할 필요는 없습니다. 임상적으로 가장 중요한 점은, 이 두 질환이 모두 배제적 진단이 필요하다는 사실이며 신경학적 신체검사만으로 말초나 중추 병변 위치를 단정하는 데에는 한계가 있으므로 ① 중이·내이 질환, ② 중추성 병변, ③ 외상 및 전신성 신경 질환을 영상검사를 토대로 순서대로 배제해야 합니다. 결국 임상에서 중요한 것은 전정 증상이나 안면신경 마비를 보이는 환자를 평가할 때, 병변이 말초성인지 중추성인지, 진행성 경과를 보이는지, 그리고 다른 신경학적 이상이 동반되는지를 단계적으로 판단하는 것입니다. 이러한 접근은 과도한 예후 비관이나 불필요한 치료를 줄이고, 보호자에게 보다 명확하고 일관된 치료 방향을 제시하는 데 도움을 줄 것입니다. 참고문헌 Garosi L, Lowrie M. Canine idiopathic vestibular syndrome. Vet Clin North Am Small Anim Pract. 2013. Bongartz U, Nessler JN, Maiolini A, et al. Vestibular disease in dogs: association between neurological examination and MRI findings. J Small Anim Pract. 2019. Schunk KL, Averill DR. Vestibular syndrome in dogs. J Am Vet Med Assoc. 1983. Jeandel A, Thibaud JL, Blot S. Facial and vestibular neuropathy of unknown origin in 16 dogs. J Small Anim Pract. 2016. Kern TJ, Erb HN. Facial neuropathy in dogs and cats: 95 cases (1975–1985). J Am Vet Med Assoc. 1987. Rossmeisl JH, Rohleder JJ, Pickett JP, et al. Reliability of neurologic examination for localization of vestibular dysfunction in dogs. Vet Clin North Am Small Anim Pract. 2010. Bongartz U, et al. Reliability of interpretation of neurologic examination findings for vestibular localization. J Small Anim Pract. de Lahunta A, Glass E. Veterinary Neuroanatomy and Clinical Neurology. Evans HE, de Lahunta A. Comparative Veterinary Anatomy: A Clinical Approach. 2022. Penderis J. Common cranial nerve disorders in dogs and cats. In Practice. Smith PM, Gonçalves R, McConnell JF. Sensitivity and specificity of MRI for detecting facial nerve abnormalities in dogs. Vet Rec. 2012. Varejão ASP, et al. Magnetic resonance imaging of the intratemporal facial nerve in idiopathic facial paralysis in dogs. Vet Radiol Ultrasound. 2006. McGregor O, Lamb CR, Targett MP, et al. Magnetic resonance imaging of the caudal digastric muscle in canine idiopathic facial neuropathy. Vet Radiol Ultrasound. 2021. Cerda-Gonzalez S, et al. Cerebrospinal fluid analysis lacks diagnostic specificity in dogs with vestibular disease. BMC Vet Res. 2020. Maiolini A, et al. Inner ear fluid-attenuated inversion recovery MRI signal intensity in dogs with vestibular disease. Vet Radiol Ultrasound. 2014. Lowrie M, Garosi L. Current definition, diagnosis, and treatment of canine idiopathic vestibular syndrome. Vet Rec. 2016. de Lahunta A, Glass E, Kent M. The neurology of balance: function and dysfunction of the vestibular system in dogs and cats. Vet Clin North Am Small Anim Pract. 2015. Cummings JF, de Lahunta A. Acute canine idiopathic polyneuropathy. Vet Clin North Am Small Anim Pract. 1978.
관리자 2026.02.04 -
 강아지 설사 기력저하 식욕 저하 - 다발성 림프종
강아지 설사 기력저하 식욕 저하 - 다발성 림프종
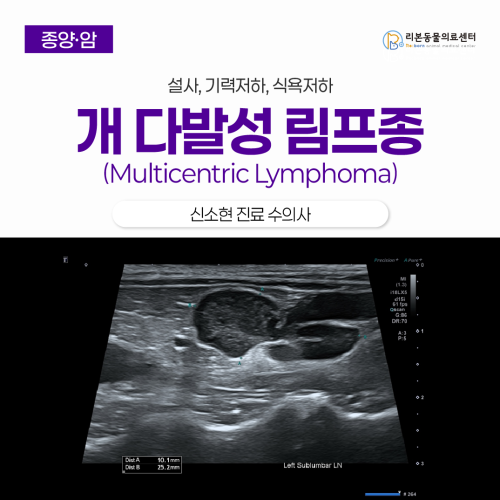
✅ 본문 한 눈에 보기 ✅ 설사와 기력 저하로 내원하여 초음파와 세포 검사(FNA)를 진행한 결과, 비장과 림프절 전반에 퍼진 다발성 림프종으로 확진되었습니다. ✅ 수술이 어려운 전신 종양 특성상 CHOP 항암 프로토콜(다약제 병용 요법)을 통해 종양 크기를 줄이고 삶의 질을 높이는 치료를 시작했습니다. ✅ 항암 시 약 1년 정도의 생존 기간을 기대할 수 있으며 치료 중 발생할 수 있는 백혈구 감소나 부작용 모니터링을 위한 정기적인 혈액 검사가 필수적입니다. 어떤 증상으로 내원했나요? 11살 중성화 수컷 개 환자가 설사, 기력저하, 식욕저하 증상을 보여 내원했습니다. 보호자님께서는 최근 들어 환자가 평소보다 많이 처져 있고, 밥을 잘 먹지 않으며 설사가 지속되어 걱정하셨습니다. 진단 과정 환자의 전신 상태 이상 원인을 확인하기 위해 복부 초음파 검사 및 세포 검사를 진행했습니다. 복부 초음파 검사 체표 및 복강 내 다발성 림프절 비대 확인 비장에서 벌집 징후(honeycomb sign) 관찰 → 종양에서 특징적으로 보일 수 있는 소견 세침 흡인 검사(FNA) 비대된 림프절에서 채취한 세포 검사에서 림프종(lymphoma) 소견 확인 위 검사 결과를 종합했을 때, 환자는 개의 다발성 림프종으로 진단되었습니다. 그림 1. 복부 초음파에서 확인된 요추하 림프절 비대 그림 2. 비장의 벌집 징후(honeycomb sign) 그림 3. 림프절의 FNA 세포검사 소견으로 림프종 진단 개의 다발성 림프종이란? 림프종은 림프구에서 발생하는 종양으로, 개에서 비교적 흔하게 발생하는 혈액·림프계 종양입니다. 다발성 림프종의 경우 림프절뿐만 아니라 비장, 간, 골수, 위장관 등 여러 장기를 동시에 침범할 수 있어 전신 증상(무기력, 식욕저하, 설사 등)이 나타날 수 있습니다. 치료 과정 및 예후 림프종은 수술만으로 완치를 기대하기 어렵기 때문에, 항암치료가 표준 치료법입니다. 증상이 있는 림프종의 환자에서 항암치료를 진행하지 않을 경우 1개월, 스테로이드 단독으로 적용할 경우 1~3개월, 다약제성 항암치료를 적용할 경우 약 1년 정도의 예후 기간을 예상할 수 있습니다. 환자 또한 다약제성 항암치료(CHOP protocol)를 적용하여 치료를 시작하기로 하였습니다. ▷ CHOP protocol 구성: Cyclophosphamide, Doxorubicin, Vincristine, Prednisolone 이 치료는 서로 다른 기전을 가진 항암제를 순차적으로 사용하여 종양 반응률을 높이고 약물 내성을 줄이는 것을 목표로 합니다. 림프종은 항암치료에 비교적 반응이 좋은 종양으로, 적절한 치료 시 임상 증상 개선과 삶의 질 향상을 기대할 수 있습니다. 다만 개체별 반응 차이가 있으며, 완치보다는 관해(remission) 유지를 목표로 치료를 진행하게 됩니다. [항암치료 중 모니터링 및 주의사항] 항암치료 중에는 호중구감소증이 나타날 수 있으므로, 정기적인 혈액검사(CBC)가 필요합니다. 일시적으로 식욕저하, 구토, 설사, 백혈구 감소 등이 발생할 수 있습니다. 그러나 무기력, 발열, 심한 식욕부진, 지속적인 설사 또는 구토가 나타날 경우 즉시 내원이 필요합니다. [가정 관리 및 보호자 안내] 치료 기간 동안 아이의 식욕, 활력, 배변 상태를 면밀히 관찰해 주세요. 항암제 투여 일정은 치료 효과에 매우 중요하므로 예약 날짜를 꼭 지켜주세요. 항암치료의 목적은 환자가 가능한 한 편안하고 질 좋은 일상생활을 유지하도록 돕는 것입니다. 궁금한 점이나 걱정되는 변화가 있을 경우 언제든 병원으로 문의해 주세요.
관리자 2026.02.03 -
 고양이 구토·식욕부진의 원인, 급성 신손상(Acute Kidney Injury, AKI)
고양이 구토·식욕부진의 원인, 급성 신손상(Acute Kidney Injury, AKI)
고양이의 반복적인 구토와 식욕부진은 급성 신손상(AKI), 위장관 질환, 전신 질환의 신호일 수 있습니다. 리본동물의료센터는 24시간 진료 체계에서 정확한 검사와 내과 분과 진료를 통해 원인을 평가합니다. [본문 한 눈에 보기] ✅ 식욕 저하, 무기력, 구토 증상으로 내원한 노령 고양이에서 중증 질소혈증과 탈수가 확인되었습니다. ✅ 혈액검사, 뇨검사, 영상검사를 종합하여 급성 신손상(AKI)으로 진단하였습니다. ✅ 본원에서 입원 정맥 수액 치료와 전해질·요독 관리, 항구토 및 위장관 보호 치료를 시행하였으며 신장 수치와 전신 상태가 점진적으로 호전되었습니다. 어떤 증상으로 내원했나요? 13세 중성화 암컷 코리안숏헤어 환자는 최근 갑작스러운 식욕 저하와 무기력, 간헐적인 구토를 보이며 내원하였습니다. 진단 과정 고양이에서 구토와 식욕부진이 갑작스럽게 나타날 경우 탈수, 신장 기능 저하, 전신 질환 가능성을 함께 고려해야 합니다.보호자 문진과 신체검사 소견을 바탕으로 급성 전신 상태 악화의 원인을 평가하기 위한 검사를 진행하였습니다. 신체검사 : 6-7 % 탈수 소견 혈액검사: BUN 151, Crea 9.4 로 심한 질소혈증 확인되었습니다. 뇨검사: USG 1.015, UPC 0.12, 도말상 감염의 소견은 확인되지 않았습니다. x-ray 검사상 특이소견은 확인되지 않았습니다. 복부 초음파 양측 신장의 퇴행성 변화 관찰되며, 신우확장 및 비뇨기 폐색 소견은 확인되지 않았습니다. 혈액검사상 급격한 신장수치 상승, 영상에서 확인되는 신장 실질의 변화와 급작스럽게 발현된 임상증상을 종합하여 본 환자는 급성 신손상(Acute Kidney Injury, AKI) 상태로 판단하였습니다. 입원치료 및 경과 입원 초기 치료의 목표는 다음과 같았습니다: 탈수 교정 및 신장 관류 회복 요독 물질 감소 전해질·산염기 불균형 교정 추가적인 신장 손상 예방 항구토 및 위장관보호 처치 이를 위해 정맥 수액 치료를 중심으로 치료를 시작하였고, 구토 조절을 위한 항구토제, 위장관 보호제를 병행하였습니다. 신장수치 및 전해질 불균형 매일 모니터링 진행하였으며, 과도한 수액으로 인한 부작용을 주의 깊게 관찰하였습니다. 입원치료를 시작함과 동시에 Cr과 BUN 수치의 점진적인 감소가 확인되었고 식욕도 서서히 회복되어 자발적인 섭식이 가능해졌습니다. 입원 기간 동안 원활한 배뇨 확인되어 환자는 무사히 보호자의 품으로 돌아가게 되었습니다. 고양이의 급성 신손상(AKI)란? 급성신손상(Acute kidney injury)는 짧은 시간 내에 신장 기능이 급격히 저하되는 상태를 의미합니다. 정상적으로 노폐물을 배출하고 체액 및 전해질 균형을 유지해야 할 신장이 갑자기 기능을 잃으면서, 혈액 내 질소 노폐물(BUN, Creatinine)이 빠르게 상승하고 전신 증상이 동반됩니다. 주요 임상 증상으로는 식욕부진, 구토, 무기력, 음수·배뇨 변화, 탈수 등이 있으며 진행 시 요독증으로 인한 전신 증상이 심화될 수 있습니다. 노령 고양이에서는 탈수, 약물, 저혈압, 감염, 요로 폐색, 패혈증 등 다양한 원인에 의해 발생할 수 있으며 특히 노령 고양이에서는 비교적 경미한 스트레스에도 AKI 가 촉발될 수 있습니다. 적절한 치료 시 회복 가능성이 존재한다는 점에서 만성 신부전과 구분되지만 회복 이후에 영구적인 신장 손상이 남을 수 있습니다. [IRIS AKI grading] AKI 의 중증도 평가는 IRIS라고 하는반려동물의 신장 질환에 대한 국제적인 수의학 전문가 협의체가 제시하는 가이드라인데 따라 이루어지는데 주로 Creatinine 수치 변화와 임상 경과를 기반으로 이루어지게 됩니다. 여기에 더해, 요량(무뇨, 핍뇨의 여부), 전해질 이상(특히 고칼륨혈증), 산증 여부 가 예후 평가에 중요한 요소로 작용하게 됩니다. 다만 AKI grade 는 고정된 단계가 아니고, 입원 중 수액 반응성, 요량, 신장수치의 변화 양상 등을 종합하여 치료반응과 예후를 평가하게 됩니다. AKI 이후, CKD로 진행될 수 있나요? 환자의 경우 AKI grade5 의 상태로 병원에 내원하였으나 입원 치료 이후에 혈액검사상 신장수치가 빠르게 호전될 수 있었습니다. 그렇지만 중요한 점 하나는 혈액검사상 신장수치가 좋아졌다고 해서 신장이 완전히 정상으로 돌아갔다고 말할 수는 없습니다. AKI 는 단순히 일시적으로 수치만 나빠졌다가 회복되는 병이 아니라 신장에 실제 손상을 남길 수 있는 사건입니다. 급성으로 신장이 손상되면 기능은 어느 정도 회복될 수 있지만 신장 조직의 일부는 영구적인 손상으로 남을 수 있습니다. 실제 여러 연구에서 AKI 를 겪은 고양이의 약 30-60 %에서 수개월-1년 이내에 만성 신장질환으로 진행될 수 있음이 보고되어 있습니다. AKI 이후, 꼭 필요한 관리와 모니터링 AKI 에서 회복한 아이에게 가장 중요한 것은 ‘지금 괜찮은지’ 보다 ‘앞으로 신장이 더이상 나빠지지 않도록 관리하는것’ 입니다. 이를 위해서 1-3개월 간격으로 정기적인 혈액검사, 소변검사, 혈압측정 등 추적 검사가 권장되며 이후 안정적일 경우 상태에 따라 검진 간격을 조절 할 수 있습니다. 급성 신손상(AKI)는 치료에 잘 반응하면 회복될 수 있는 질환이지만 동시에 만성 신장질환으로 이어질 수 있는 중요한 분기점이기도 합니다. 아이가 다시 예전처럼 잘 먹고 활발해 보이더라도 정기적인 검진과 모니터링을 통해 신장의 변화를 조기에 발견하는 것이 아이의 삶의 질과수명을 지키는 가장 확실한 방법입니다.
관리자 2026.01.22 -
 강아지 다리 혹 (연부조직육종 STS), 다리 종양 제거 수술 + 피부 재건 수술+ 림프절 제거
강아지 다리 혹 (연부조직육종 STS), 다리 종양 제거 수술 + 피부 재건 수술+ 림프절 제거
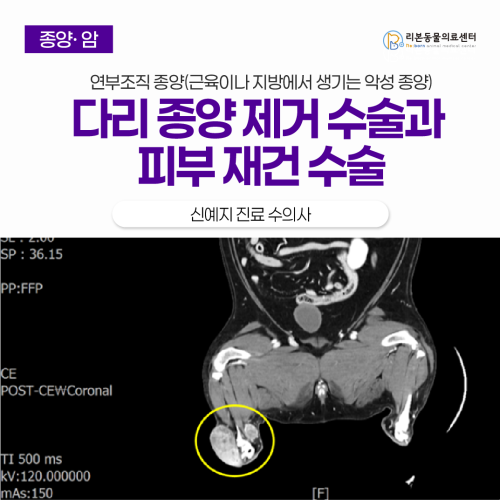
강아지를 쓰다듬다 뒷다리에서 혹이나 멍울이 만져져 걱정되신 적 있으신가요? 강아지 혹은 단순한 지방종부터 종양이나 암으로 진행되는 경우까지 원인이 다양해 크기가 커지거나 단단하게 느껴진다면 정확한 검사가 필요합니다. 이번 글에서는 강아지 뒷다리 혹으로 내원한 웰시코기 사례를 통해 종양의 진단 과정과 치료 과정을 자세히 소개드립니다. [본문 한 눈에 보기] ✅ 산책 중 웰시코기 환자는 오른쪽 뒷다리에서 점점 커지는 혹이 만져져 병원에 내원했고 검사 결과 근육이나 지방에서 자라는 종양이 확인되었습니다. ✅ CT 검사와 세포 검사로 악성 종양 가능성이 높다고 판단되었지만 종양 위치가 발에 가까워 다리를 절단하지 않고 종양만 제거하는 수술과 피부를 이어주는 수술을 진행했습니다. ✅ 수술 후 조직검사 결과에서는 비교적 초기 단계의 악성 종양으로 확인되었고 현재는 회복 중이며 재발 여부를 계속 관찰하고 있습니다. 내원 이유 보호자님과 환자가 산책 중 뒷다리에 혹 같은 덩어리를 발견하셔서 병원에 내원하셨습니다. 내원 당시 몇 달 전 처음 발견했을 때보다 많이 커진 것 같다고 하셨습니다. 진단 과정 신체검사에서 보행에 불편함은 없었으나 우측 뒷다리에 5cm*6cm 정도의 큰 종괴를 확인하였습니다. CT 촬영을 통해 해당 종양이 아킬레스건 주변을 둘러싸고 근육 침습도 일으키고 있는 양상을 확인하였습니다. 원격 전이를 의심할 만한 소견은 없었지만 인접한 림프절 중 하나인 sublumbar LN(요추하 림프절이 커져 있었습니다. FNA(미세침흡인검사)는 농양 등 종양의 다른 원인을 배제하거나 종양의 종류를 유추하는 데 사용할 수 있습니다. 다만, 중간엽세포 유래 종양의 경우 세포가 잘 탈락하지 않아 진단률은 떨어지는 편입니다. 그럼에도 수술적 절제 전 종양의 특성을 대략적으로 확인하고 수술적 계획을 세우는 데 도움이 됩니다. FNA 검사 결과 sarcoma계열 종양이 가장 강하게 의심되는 소견이 나왔습니다. 치료 계획 종양의 치료는 결국 수술적 절제인데 수술의 목표는 여러 가지로 나뉩니다. 완전 절제를 통한 치료 목적, 종양의 일부 절제를 통한 세포 수 감소 목적, 종양이 주변 장기 등을 눌러 임상 증상을 유발하는 경우 임상 증상 완화의 목적, 조직 검사를 위한 일부 조직 생검의 목적 등입니다. FNA를 통해 의심되는 Sarcoma(육종)는 악성 종양이며 크기도 5cm 이상으로 매우 크고 주변 근육 침습도도 높아 완전 절제를 위해서는 종양 주변 3cm 이상의 넓은 margin(변연)을 두고 절제해야 완전 절제와 치료를 기대할 수 있습니다. 그러나 사지 말단에 위치하여 주변 조직과 피부가 부족하여 넓은 변연을 확보할 수 없습니다. 따라서 치료적 목적을 위해서는 amputation 즉 해당 병변이 위치한 다리 절단이 필요합니다. 사지 절단 후 연구에서 약 90%의 보호자들은 강아지들이 절단 전후 큰 변화 없이 잘 적응했다고 응답했습니다. (2015, Vanna) 그렇지만 보호자께서 이후 재발 가능성이 높더라도 종양의 marginal한 절제만 시행하기를 강하게 원하셨습니다. 해당 종양은 너무 커서 marginal하게 시행하더라도 봉합을 위한 피부 조직이 모자라 주변 피부를 끌어오는 axial pattern flap을 시행하기로 계획을 세웠습니다. genicular axial pattern flap 수술: STS resection Marginal resection이지만 주변 피부가 허락하는 한 넓은 면적을 절제하였습니다. 절제하면서 popliteal LN도 함께 절제했습니다. 종양을 제거하는 모습 절제한 종양 이후 genicular axial pattern flap을 통해 주변 피부를 가져와 봉합했으며 복강경을 통해 sublumbar LN을 제거하여 술후 통증과 합병증을 최소화하고자 했습니다. Flap을 통해 피부 조직을 닫으려는 모습 피부 봉합이 완료된 후 모습 입원 관리 및 예후 입원 기간 동안 철저한 감염 관리와 통증 관리를 진행했습니다. Flap을 통해 주변 조직을 이식한 것이기 때문에 일반적인 봉합보다 회복이 더디고 감염에 취약합니다. 주변 조직을 당겨오며 발생하는 장력 때문에 열개가 쉽게 생길 수 있어 매일 술부를 모니터링했습니다. 환자는 입원 기간 동안 큰 이상 없이 지내다가 퇴원했습니다. 퇴원 후에도 지속적인 재발 유무를 모니터링하기로 했습니다. 조직 검사 조직 검사 결과 grade I STS로 진단되었습니다. 사지 말단의 종양이라는 위치적 한계 때문에 절제 단면까지 종양이 있어 추가적인 재발 여부를 계속 모니터링해야 합니다. 그리고 만약 재발한다면 더욱 공격적인 양상을 띌 가능성이 높아 절단을 고려해야 합니다. 다행히도 커져 있던 림프절들에는 전이의 증거가 없었습니다. 질병 소개: STS (Soft tissue sarcoma) Soft tissue sarcoma (STS), 연부조직육종은 개의 피부 종양에서 약 8-15% 고양이에서는 7-18%를 차지하는 악성 종양입니다. 다양한 중간엽 기원 세포에서 발생하지만 생물학적 행동의 유사성 때문에 하나의 그룹으로 분류합니다. 주변과 피막으로 잘 분리되어 보이지만 미세한 돌기 형태로 침윤하여 침습적인 성장 양상을 보이며 때문에 marginal 하게 절제한 경우 재발이 흔하게 발생합니다. 종양에서 중요한 분류로 Staging과 Grading이 있습니다. Staging은 종양의 크기, 림프절 전이, 원격 전이 등 종양의 성장과 전파와 관련된 등급을 매긴 것으로, 평균 생존 기간 분류에 사용되는 경우가 많습니다. Grading은 조직 검사를 통해 조직학적/세포학적으로 얼마나 비정상적인지 악성도가 높은지 등급을 매긴 것입니다. 둘 모두 예후와 관련이 깊은 지표입니다. 특히 grading은 원격 전이와 국소 재발을 모두 예측할 수 있기 때문에 치료 방향 설정과 모니터링을 위해 종양 절제 후 조직 검사는 필수적입니다. STS의 전이률은 Grade에 따라 크게 달라집니다. 저등급 STS(grade I, II)에서는 13%이하로 보고되었고 고등급 STS(grade III)에서는 44%까지 보고되었습니다. 가장 흔한 전이 장기는 폐입니다. 이런 원격 전이는 예후에 큰 영향을 미치기 때문에 전이 평가를 위한 CT가 필요합니다. 유일한 치료 방법은 수술적 절제술입니다. 종괴로부터 3cm 이상, 하나 이상의 정상 근막을 포함하는 가급적 넓은 margin을 확보해야 하는데 몸통처럼 주변 조직이 많은 부위에선 가능할 수 있어도 사지 말단부에서는 거의 불가능하여 amputation이 추천됩니다. 완전 절제만 된다면 치료율은 매우 높아집니다. 그러나 변연이 좁거나 불완전한 경우 STS는 국소 재발률이 7-35%로 매우 높은 편입니다. 특히 grade에 따라 재발률이 크게 달라지는데 grade I에서는 7%, grade II에서는 35%, grade III에서는 75%까지 나타났습니다 (2009, Mcsporran). 재발한 STS는 더 공격적이고 예후가 나쁜 경향을 나타냅니다. 따라서 좁거나 불완전한 변연이 확인되었다면 scar revision을 통한 재수술 혹은 방사선 치료를 통해 재발을 줄이는 것이 추천됩니다. 특히 grade III STS의 경우 높은 전이도 때문에 수술 후 추가적인 방사선 치료 또는 항암 치료가 권장됩니다. 보호자님께 드리는 말씀 아이를 쓰다듬거나 만져 주실 때 이전에 없던 덩어리가 만져지는 경우 병원에 내원하여 검사를 받아 보시는 편이 좋습니다. 모든 STS가 그런 것은 아니지만 대부분의 경우 말랑말랑한 지방종보다는 딱딱한 느낌의 덩어리를 만질 수 있습니다. 주변 조직 침습도도 높고 빠르게 자라는 종양이기 때문에 확인된다면 바로 제거가 추천되며 가능한 넓게 절제해야 재발을 막을 수 있습니다. 추천되는 3cm 이상의 변연을 위해서 사지 말단에 위치한 경우 절단까지 고려해 주셔야 합니다. STS의 특징 중 하나는 재발 시 더 공격적으로 변한다는 점입니다. 가급적 첫 수술에 넓고 완전한 절제를 하는 것이 가장 좋은 예후를 기대할 수 있습니다. 강아지 혹 특히 뒷다리나 사지에 생긴 종양은 위치와 크기에 따라 치료 방법과 예후가 크게 달라질 수 있습니다. 혹이 빠르게 커지거나 단단하게 만져진다면 단순한 문제로 넘기지 말고 CT 검사와 조직 검사를 통해 정확한 진단을 받는 것이 중요합니다. 리본동물의료센터는 강아지 종양에 대해 정확한 영상 검사와 수술적 치료, 수술 후 재발 관리까지 체계적으로 진행하고 있습니다. 아이의 혹이나 멍울로 고민 중이시라면 가까운 동물병원 또는 리본동물의료센터로 상담 (051-711-0006) 받아보시기 바랍니다. 감사합니다.
관리자 2026.01.07 -
 강아지 씨앗 삼킴, 강아지 구토, 소장 이물 제거술 - 장 절개술 (Enterotomy)
강아지 씨앗 삼킴, 강아지 구토, 소장 이물 제거술 - 장 절개술 (Enterotomy)
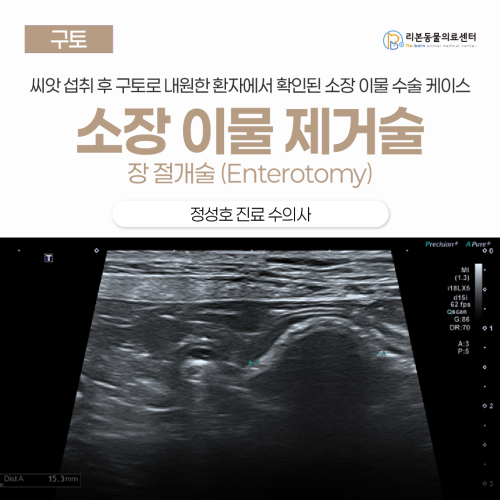
강아지 씨앗 삼킴, 강아지 구토, 소장 이물 제거술 - 장 절개술 (Enterotomy) 강아지가 갑자기 구토를 반복하고 보호자 몰래 뭔가를 먹은 것 같을 때 “이물질 먹은 걸까요?” “사람 음식 먹은 것 같아요” “조금 더 지켜봐도 될까요, 바로 병원 가야 하나요?” 이런 고민으로 검색을 하게 됩니다. 강아지 구토는 비교적 흔한 증상이지만 이물 섭취로 인한 소장 폐색이 원인인 경우에는 단순한 위장염과 달리 지체하면 위험해질 수 있는 응급 질환일 수 있습니다. 직접 이물 섭취를 보지 못했음에도 정밀 검사 후 소장 이물이 확인되어 수술로 치료한 실제 케이스를 바탕으로 보호자님이 꼭 알고 계셔야 할 진단 과정과 판단 기준을 설명드리기 위해 작성되었습니다. [본문 한 눈에 보기] ✅ 2–3일간 반복적인 구토로 내원한 환자로 문진과 검사상 전신 질환보다는 위장관 문제 가능성이 의심되었습니다. ✅ 방사선 검사만으로는 확진이 어려워 복부 초음파를 시행했고 회장 부위 소장 이물을 확인하여 수술 진행했습니다. ✅ 장 괴사 소견은 없어 장 절개술로 이물을 제거했으며 조기 수술로 합병증 위험을 낮추고 예후는 양호했습니다. 내원한 이유 이번 환자는 2–3일 전부터 반복적인 구토를 보여 내원한 케이스였습니다. 제목을 보고 오신 분이라면 이미 이 환자의 원인이 ‘이물’임을알고 계시겠지만 수의사 입장에서는 구토만으로 곧바로 이물을 단정할 수는 없습니다. 구토는 동물병원에서 가장 흔히 접하는 증상 중 하나이며 원인이 매우 다양합니다. 심지어 보호자가 “구토를 한다”고 내원했지만 실제로는 역류를 구토로 오인 경우도 적지 않습니다. 따라서 구토를 주증로 내원한 경우 철저한 문진이 진단의 출발점이 됩니다. 이 환자 역시 구토가 시작된 시점과 빈도, 토사물의 형태(사료, 담즙, 이물 등),식이 변경 여부,이물 섭취나 사람 음식 섭취 이력 등을 세밀히 확인했습니다. 보호자 말씀으로는 최근 식이 변화나 이물, 사람 음식 섭취는 없었다고 하셨습니다. 진단 신체검사를 이어서 진행했습니다. 촉진시 복부에 뚜렷한 불편감을 보였고 소화기 내 가스 팽창이 손끝으로 느껴졌습니다. 이러한 경우에는 우선적으로 혈액검사를 통해 구토를 일으킬 수 있는 전신적·대사성질환(non-GI질환)을 감별해야 합니다. 특히신장 질환, 간 질환, 췌장염 등은 구토의 주요 원인들입니다. 이 환자의 경우, 신장 수치,간수치, 췌장 관련 수치 모두 정상 범위로 확인되었습니다. 따라서, 전신 질환보다는 위장관 자체의 문제 가능성을 우선적으로 고려하게 되었습니다. 하지만 이러한 소견은 구토를 유발하는 다양한 질환에서 공통적으로 관찰될 수 있는 비특이적 변화이기에 이것만으로 질병을 특정할 순 없었습니다. 보호자분은 문진 시 환자가 이물을 삼키는 것을 직접 보지 못했다고 말씀하셨지만 문진만으로 이물이나 기계적 폐색을 배제할 수는 없습니다. 반려동물이 보호자 몰래 이물을 삼키는 경우가 흔하기 때문입니다. 따라서, 구토의 흔한 원인 중 하나인 이물 가능성을 우선적으로 확인하는 과정이 필요합니다. 이럴 때는 기계적 폐색(이물로 인한 장 막힘) 여부를 확인하기 위해 접근성이 좋고 신속하게 진행할 수 있는 복부 방사선(X-ray) 검사를 먼저 시행하는 것이 일반적입니다. 하지만 방사선 검사는 이물 진단의 민감도와 특이도가 약 66% 수준으로 단독으로는 정확도가 높지 않습니다. 실제로 이 환자의 경우, 방사선상 씨앗 형태의 이물로 의심되는 희미한 음영이 관찰되었으나 음영이 뚜렷하지 않았고 소장의 명확한 확장 소견도 확인되지 않아 단순 방사선만으로는 이물에 의한 폐색을 확정하기 어려운 상황이었습니다. 따라서 이런 경우에는 복부 초음파 검사를 추가로 시행하여 이물 자체의 위치와 형태, 장벽의 두께 변화, 장 운동성, 폐색 부위 전후의 확장 정도 등을 평가함으로써 진단의 정확도를 높이는 것이 필요했습니다. 확실한 진단을 위해 복부 초음파 검사를 진행했습니다. 초음파 검사상회장(ileum) 부위에서 소장 내 이물이 명확히 확인되었습니다. 수술 소장 이물 수술은 장 절개술(enterotomy) 또는 장 절제·문합술(enterectomy& anastomosis)로 진행됩니다. 이물은 장을 압박해 혈류를 방해하고 장벽에 허혈성 손상을 유발할 수 있습니다. 따라서 장벽의 괴사 여부가 수술 방법 선택의 핵심 기준이 됩니다. –괴사가 없는 경우: 장을 절개하여 이물만 제거(장 절개술) –괴사가 있는 경우: 손상된 장분절을 절제하고 건강한 부위를 서로 이어주는 문합술시행 이 환자의 경우 개복 후 괴사여부 판단을 위해서,소장의 색깔, 연동운동 유무, 장간막혈관의 박동, 장절개시 출혈 반응 등을 종합적으로 평가했습니다. 그 결과, 장 괴사 소견은 없었기 때문에 장 절개술만으로 이물을 안전하게 제거할 수 있었습니다. 소장이물 수술을 지연하면 안되는 이유 (1) 보호자분들 중에는 “씨앗 좀 먹었다고 큰일이 나겠어요?”, “조금 기다리면 변으로 나오지 않나요?” 라고 생각하시는 분들도 계실 겁니다. 물론, 일부 이물은 자연 배출되기도 합니다. 하지만장의 어디에 어떤 형태로 걸렸는지에 따라 상황은 전혀 달라집니다. 2021년 VeterinarySurgery저널에 발표된 연구에 따르면 수술을 지연한 경우 장 괴사와 천공 발생이 유의하게 많았으며 이로 인해 장 절제 및 문합술이 필요한 비율이 증가했습니다. 또한, 마취 및 수술 시간 역시 지연군에서 더 길었다고 보고되었습니다. 즉, 단순히 “기다려보자”는 선택이 결국엔 더 큰 수술과 위험으로 이어질 수 있다는 점을 반드시 인지해야 합니다. 소장이물 수술을 지연하면 안되는 이유 (2) 수술을 미루다 발생할 수 있는 장 천공이 얼마나 위험한지 실감이 나지 않는 분들을 위해 객관적인 연구 결과를 하나 소개드리겠습니다. 2011년 JAVMA에 발표된 연구에 따르면 수술 전 이미 장 천공으로 인해 세균성 복막염이 발생한 경우 수술 후 사망률이 33%에 달했습니다. 반면, 천공이 발생하지 않은 상태에서 이물 수술한 경우의 사망률은 11%에 불과했습니다. 즉, 장 천공이 동반되면 사망 위험이 세 배 이상 증가한다는 뜻입니다. 소장이물 수술을 지연하면 안되는 이유 (3) 앞서 말씀드렸듯이 수술이 지연될수록 장문합술을 해야 하는 비율이 높아집니다. 그리고 실제로 장문합술을 시행한 경우와 단순 장절개술로 끝난 경우의 예후 차이를 비교한 연구도 있습니다. 2021년 JAVMA에 발표된 연구에 따르면, 장절개술(enterotomy)을 시행한 경우 장열개(dehiscence) 발생률은 3.8%, 장문합술(enterectomy& anastomosis)을 시행한 경우는 18.2%였습니다. 즉, 장문합술을 시행한 경우 장열개가 발생할 가능성이 약 6배 이상 높았던 것입니다. 이 연구의 핵심은 “장문합술이 위험하니 하지 말자”는 의미가 아닙니다. 오히려 장문합술까지 필요할 정도로 장 손상이 진행된 경우 이미 예후가 나빠져 있다는 사실을 보여주는 것입니다. 따라서, 수술을 지연하면 할수록 장 손상이 심해지고 결국 더 큰 수술과 높은 합병증 위험으로 이어질 수 있음을 명심해야 합니다. 합병증 장열개(dehiscence) :앞서 말씀드렸듯이, 장 절개술(enterotomy)의 경우 장열개(dehiscence) 발생률은 약 3.8%, 장문합술(enterectomy& anastomosis)의 경우는 18.2%로 보고되었습니다. 이러한 장열개는 복막염(peritonitis)을 유발하고 전신 염증 반응(SIRS)으로 진행될 수 있어 예후를 급격히 악화시키는 주요 합병증입니다. ileus(장마비) :ileus(장마비)는 장을 직접 조작하는 수술의 특성상 비교적 흔하게 발생할 수 있습니다. 따라서 수술 후 이물이 완전히 제거되었더라도 일시적인 장운동저하로 인해 구토 등 소화기계 임상 증상이 다시 나타날 수 있습니다. 이러한 경우에는 대부분 시간이 지나면서 장 기능이 회복되지만 초기에는 세심한 모니터링과 보조적 치료가 필요합니다. 예후 이물을 제거한 후의 전반적인 예후는 양호하며 보고된 사망률은 대체로 1–8% 수준입니다. 다만, 여러 부위에서 장 절개가 필요한 경우나 광범위한 소장 절제 및 장문합술을 시행해야 하는 경우에는 수술 범위가 넓어지고 합병증 위험이 증가하기 때문에 예후가 상대적으로 불량해질 수 있습니다. ✔하루 이상 구토를 반복하거나 ✔물을 마셔도 바로 토하고 ✔배를 만질 때 통증이나 불편 반응을 보이거나 ✔보호자 몰래 무언가를 먹었을 가능성이 있다면 단순한 위장 트러블로만 넘겨서는 안 됩니다. 이런 경우에는 이물로 인해 장이 막혀 있는 상황은 아닌지 반드시 확인하는 과정이 필요합니다. 이물로 인한 장 폐색은 처음에는 단순 구토처럼 보일 수 있지만, 시간이 지날수록 장의 혈류 장애와 손상이 진행될 수 있으며 진단이 늦어질 경우 수술 범위가 커지고 합병증 위험 또한 크게 증가할 수 있습니다. 강아지 구토가 계속되고 이물 섭취가 의심된다면 지켜보는 시간보다 정확한 검사와 판단을 먼저 받는 것이 아이의 회복과 예후를 결정짓는 중요한 선택이 됩니다.
관리자 2026.01.06
Re:born ANIMAL MEDICAL CENTER





